Subscribe to get access
Read more of this content when you subscribe today.
Read more of this content when you subscribe today.
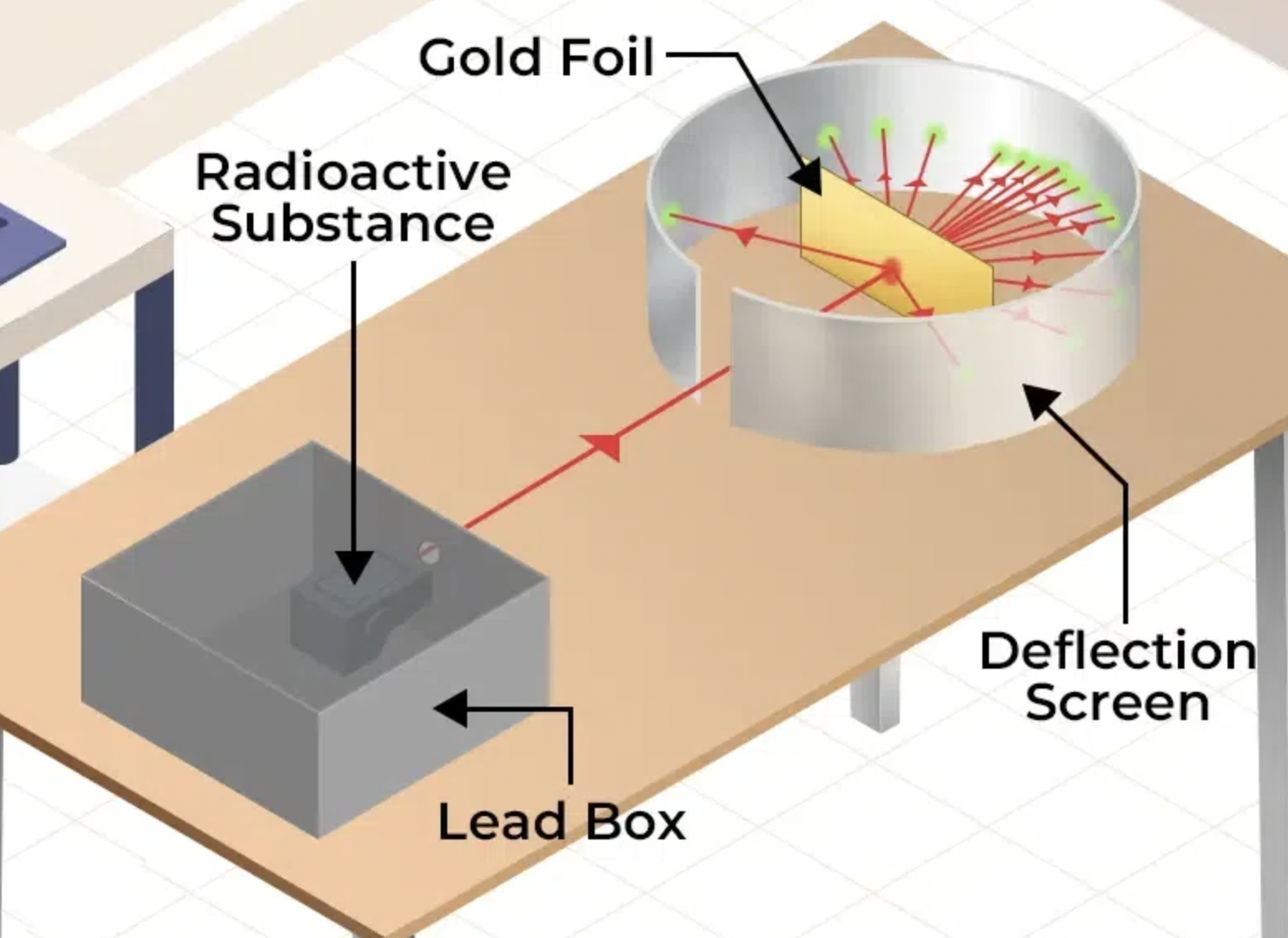

ஆல்பா துணிக்கைகளை வெளிப்படுத்தும் கதிர்வீச்சு பகுதிக்கும் அவை ஊடுருவிச் செல்லக் கூடிய விதத்தில் நாக சல்பைட்டால் ஆன திரைக்கும் (fluorescent screen) இடையே தங்கத்தினால் ஆன மெல்லிய திரை ஒன்று வைக்கப் பட்ட போது அதை ஊடுருவாது திசை திருப்பப் பட்ட ஆல்பா கதிர்களின் அளவு நுணுக்குக் காட்டியால் நோக்கப் பட்டது.
இதன் போது தோம்சனின் பிளம் புட்டிங் மாதிரிப்படி அணு முழுக்க பரவிய மின்சார மேகம் போல இருக்குமென நம்பினர். ஆகவே அனைத்து ஆல்பா துகள்களும் நேராகச் செல்லும் என நினைத்தார்கள். அணு பெரும்பாலும் வெற்றிடமாக இருப்பதால் பெரும்பாலான ā ஆல்பா கதிர்கள் நேராகச் சென்றது. சில துகள்கள் விலகிச் சென்றன. இதற்கு உள்ளே பாஸிட்டிவ் திணிவு இருப்பது கருதப் பட்டது. மிக மிகக் குறைவான துகள்கள் வெளியிலிருந்து சுவரில் மோதியபடி திரும்பி வந்தது. இது சாத்தியமாகும் மிகச்சிறிய மிக நெருக்கமான மிக அதிக பாஸிட்டிவ் சார்ஜ் உள்ள மையம் இருந்தால் தான் என பின்னர் விளக்கம் பெறப்பட்டது. இதனால் தோம்சனின் பிளம் புட்டிங் மாடல் கைவிடப் பட நேர்ந்தது.
பின்னர் பெறப்பட்ட ரதர்போர்டின் மாதிரியில் அணுவின் மையத்தில் நெருக்கமாக இருக்கும் பாஸிட்டிவ் திணிவு நியூக்ளியஸ் Nucleus எனப்பட்டது. மேலும் அணுவின் பெரும்பாலான இடம் வெற்றிடம் என்றும் இந்த நியூக்ளிய̀ஸை சுற்றி எலெக்ட்ரான்கள் அமைந்துள்ளன என்றும் முடிவுகள் பெறப்பட்டன. ஆனாலும் அதன் பின வேதியியலில் ரதர்போர்டின் மாதிரியிலும் திருத்தங்கள் மேற்கொள்ளப் பட்டு போரின் மாதிரி ஏற்றுக் கொள்ளப் பட்டது.
ரதர்போர்டின் அணு மாதிரி பெரும்பாலும் நமது சூரிய குடும்பத்தின் உருவமைப்புடன் ஒப்பிடப் பட்டே விளக்கப் பட்டது. சூரிய குடும்பத்தின் மிகப் பெரும் பகுதி வெற்றிடமாக இருப்பது போல் அணுவின் உள்ளேயும் மிகப் பெரும் பிரதேசம் வெற்றிடமாக உள்ளது. சூரிய குடும்பத்தில் சூரியன் போன்று நியூக்ளியஸும், கிரகங்களைப் போன்று எலெக்ட்ரான்களும் அமைந்திருப்பதாக விளக்கப் பட்டது. ஆனால் ஒரு முக்கிய வேறுபாடு இருந்தது. சூரியக் குடும்பத்தில் கிரகங்கள் ஈர்ப்புச் சக்தியால் நிலைக்கின்றன. ஆனால் எலக்ட்ரான்கள் positive நியூக்ளியஸைச் சுற்றி சுற்றினால், அவை மின்னியல் கதிர்வீச்சு (electromagnetic radiation) வெளியிட வேண்டும். இதனால் ஆற்றலை இழந்து வட்டம் குறைந்து நியூக்ளியஸில் விழ வேண்டும்.
ஆனால் அவ்வாறு நடப்பதில்லை. இதனால் ரதர்போர்டு மாதிரி முழுமையாகச் சரியானது அல்ல. இதன் பின்னர் வந்த அறிவியலாளரான நீல்ஸ் போர் வெளிப்படித்திய மாதிரி இந்தப் பிரச்சினையைச் சரி செய்தது. அவரது முக்கியமான கண்டுபிடிப்பு எலெக்ட்ரான்கள் குறிப்பிட்ட நிலையான ஆற்றல் படிநிலைகளில் (Energy Levels) இல் மட்டுமே இருக்கலாம் என்பதாகும்.
கெய்கர் மாடிசன் இருட்டறையில் தங்க தகட்டினால் திசை திருப்பப் பட்ட ஆல்பா கதிர்களை வெறும் கண்னால் நோக்கி சிரமப் பட்ட நிலையில் இன்று அணுக்கரு மற்றும் அடிப்படைத் துகள்களைக் கண்டறிவத்ற்கான சிதறல் பரிசோதனைகள் மிகவும் சிக்கலானதாகவும் கணணி வாயிலாகப் பதிவுகளை எடுத்து ஆய்வு செய்யக் கூடியவையாகவும் வளர்ச்சி அடைந்துள்ளது. எலெக்ட்ரோனிக் கண்டுபிடிப்பான்கள் மூலம் துணிக்கைகள் இனம் காணப் பட்டு பல ஜிகாபைட் (GB) அளவுடைய தகவல்கள் கணணியில் சேகரிக்கப் பட்டு பௌதிகவியலின் முக்கிய அணு சம்பந்தமான ஆய்வுகள் இன்று சேர்ன் CERN போன்ற ஆய்வகங்களில் மேற்கொள்ளப் பட்டு வருகின்றன.
நீல்ஸ் போரின் அணுமாதிரியுடன் அணுக்கருவின் மிகச்சிறிய அளவீடுகளில் துணிக்கைகளின் இயல்பை விளங்கிக் கொள்ளக் கூடிய விதத்திலான குவாண்டம் வேதியியல் கோட்பாடு கட்டமைக்கப் பட்டது. இதில் மேக்ஸ் பிளாங்க மற்றும் அல்பேர்ட் ஐன்ஸ்டீன் ஆகிய இரு முக்கிய அறிவியலாளர்களின் பங்களிப்பு மிக முக்கியத்துவம் வாய்ந்ததாக உள்ளது.
நீல்ஸ் போர் தனது அணுக்கரு மாதிரியை (Bohr Atomic Model) உருவாக்கும்போது பயன்படுத்திய முக்கிய ஆதாரம் ஹைட்ரஜன் வாயுவின் மின்-வெளிச்ச (electric discharge) ஸ்பெக்ட்ரம் ஆகும். இது ஹைட்ரஜன் வாயுவைக் கொண்ட கண்ணாடிக் குழாயில் (discharge tube) உயர் மின்னழுத்தத்தை செலுத்தும் போது பெறப்பட்டது. எலெக்ட்ரான் ஒரு பாதையில் இருந்து மற்றொரு பாதைக்கு குதிக்கும் போது ஆற்றலை வெளியிடும் அல்லது ஏற்கும். வெளியிடப் படும் போட்டோன் (Photon) ஆற்றல் E=hν என்ற கணித சமன்பட்ட்டால் மதிப்பிடப் படுகின்றது.
அதாவது, ஹைட்ரஜனின் ஸ்பெக்ட்ரல் கோடுகள் ஏன் குறிப்பிட்டவையாக மட்டுமே உள்ளன என்பதற்கு போர் முதல் முறையாக கணிதத்துடன் சரியான பதில் கொடுத்தார். இந்த மாதிரியில் எலக்ட்ரான்களின் நிலையான ஆற்றல் நிலைகள் மற்றும் ஆற்றல் குதிப்புகள் (quantum jumps) முக்கிய பங்கு வகிக்கின்ற போதும் நீல்ஸ் போர் ஆரம்பத்தில் ரதர்போர்டின் சூரிய குடும்ப கட்டமைப்புக்கு ஒத்த கட்டமைப்பை ஏற்று ஆனால் எலெக்ட்ரான்கள் ஏன் குறித்த சக்தி மட்டங்களில் மாத்திரம் (ஆர்பிட்டரில்?) சக்தியை இழக்காது வலம் வருகின்றன என விளக்கம் அளித்தார். பின்னர் 1920 களில் குவாண்டம் பௌதிகவியல் பற்றிய புரிதல் விருத்தியடைந்த அணுக்கரு தொடர்பான புதிய கட்டமைப்பு பெறப்பட்ட போது இந்த சூரிய குடும்ப மாதிரியும் கைவிடப் பட்டது.
வேதியியலின் சில அடிப்படை அளவீடுகளைப் பார்ப்போம். அணுவொன்றில் கா̀ணப்படும் மறை ஆற்றல் கொண்ட எலெக்ட்ரோன்களின் எண்ணிக்கை அதன் மையத்தில் கருவில் (Nucleus) காணப்படும் நேர் ஆற்றல் கொண்ட துணிக்கைகளின் எண்ணிக்கைக்கு சமனாகும். இந்த எண்ணிக்கை அணுவெண் எனப் படுவதுடன் இது ஆங்கிலத்தில் Z என்ற எழுத்தால் குறிப்பிடப் படுகின்ற்து. ஒரு அணுவின் அணுவென் Z ஆனது அந்த அணு எந்த மூலகத்தைச் சேர்ந்தது என்பதைக் குறிப்பிடுகின்றது. உதாரணத்துக்கு ஹைட்ரஜனின் அணுவெண் Z = 1 மற்றும் ஹீலியம் அணுவின் அணுவெண் Z=2 ஆகும். அதாவது ஹைட்ரஜன் அணு 1 எலெக்ட்ரோன் மற்றும் 1 புரோட்டனையும், ஹீலியம் அணு 2 எலெக்ட்ரோன் மற்றும் 2 புரோட்டன்களையும் கொண்டிருக்கும்.
எமது பிரபஞ்சத்தில் அதிகளவில் காணப்படும் மூலகங்களாக ஹைட்ரஜன் மற்றும் ஹீலியம் அணுக்கள் அமைந்துள்ளன. பிரபஞ்சத்தில் இருக்கும் கண்ணுக்குத் தெரியும் சடப்பொருளில் (Matter) 3/4 பங்கு ஹைட்ரஜனும், எஞ்சியவற்றில் பெரும்பான்மை ஹீலியமும் காணப் படுகின்றது. பூமியில் இனம் காணப் பட்ட எஞ்சிய கிட்டத்தட்ட 90 மூலகங்களில் பிரபஞ்சத்தில் எஞ்சிய 2% வீதத்தையே நிரப்புகின்றன. ஆனாலும் எமது பூமி போன்ற சில பொதுவான இடங்களில் கார்பன், ஆக்ஸிஜன் மற்றும் இரும்பு ஆகியவை அதிகளவில் காணப் படுகின்றன. இந்த அரிதான மூலகங்கள் யாவும் பிரபஞ்சத்தில் அடிக்கடி நிகழும் நட்சத்திரங்களின் சூப்பர் நோவா வெடிப்புக்களின் போது தோற்றம் பெறுவதாகக் கண்டுபிடிக்கப் பட்டுள்ளது. இது தொடர்பான தகவல்களைப் பின்பு விரிவாகப் பார்ப்போம்.
ஹைட்ரஜனின் அணுக்கருக்கு ரதர்போர்டு புரோட்டன் எனப் பெயர் சூட்டினார். இதில் காணப் படும் 1 புரோட்டன் அதைச் சுற்றி ஒரு சக்தி மட்டத்தில் வலம் வரும் 1 எதிர்மறை ஆற்றல் கொண்ட எலெக்ட்ரானை விட 2000 மடங்கு அதிக எடை கொண்டிருப்பதாகவும் ரதர்போர்டு தெரிவித்தார். மேலும் ஹீலியம் அணுவில் 2 புரோட்டனுடன் புரோட்டனின் நிறைக்கு சமனான 2 நியூட்ரோனையும் அது கொண்டிருப்பதால் ஹைட்ரஜனை விட ஹீலியம் 4 மடங்கு அதிக எடை கொண்டிருப்பதாகவும் கண்டுபிடிக்கப் பட்டது. நியூட்ரோனின் ஆற்றல் பூச்சியம் என்பது குறிப்பிடத்தக்கது. புரோட்டன்கள், நியூட்ரோன்கள் மற்றும் ஐசோடோப்கள் பற்றிய சிறு அறிமுகத்துடன் குவாண்டம் வேதியல் தொடர்பான ஆய்வுக் கட்டுரையை அடுத்த வாரம் எதிர்பாருங்கள்.